Содержание
- 1 Как был открыт галлий
- 2 Понятие легкоплавких металлов/сплавов
- 3 Какие есть технологии плавления металлов в домашних условиях?
- 4 Натрий (97,8°C)
- 5 Чем опасна нехватка витамина Д?
- 6 Использование самого легкоплавкого металла в медицине
- 7 Вольфрам
- 8 Примерная программа упражнений на неделю
- 9 Оборудование и материалы, которые понадобятся
- 10 Свойства галлия
- 11 Плавка металла и чугуна
- 12 Интересные опыты с галлием
- 13 Свойства
- 14 4. Хром
- 15 Суть понятия самого легкоплавкого металла
- 16 Муфельная печь
- 17 Области применения галлия
- 18 В заключение
Как был открыт галлий
Существование галлия было предсказано Д. И. Менделеевым в 1871 на основании сформулированного им . Менделеев дал этому элементу название «экаалюминий» и предсказал у него такие свойства как плотность, температуру плавления. Также Менделеев предсказал:
- характер оксида,
- связь в соединениях с хлором.
- что металл будет медленно растворяться в кислотах и щелочах;
- он не будет реагировать с воздухом;
- оксид экаалюминия M₂O₃ должен реагировать с кислотами с образованием солей MX₃;
- что он должен образовывать основные соли;
- хлорид обладает большей летучестью, чем ZnCl₂;
- что этот элемент откроют с помощью спектроскопии.
Менделеев оказался Ностардамусом в химии: когда галлий был получен, все предсказанные ученым свойства подтвердились!
В 1875 году французский химик Поль Эмиль Лекок де Буабодран изучал сфалерит с помощью спектроскопии и обнаружил две фиолетовые линии, принадлежащие новому элементу. Год спустя ученый выделил новый элемент с помощью электролиза. Этот элемент Буабодран назвал в честь латинского названия Франции — Gallia. Существует легенда, что в это название ученый вкладывал и другой смысл. Лекок созвучно с французским le coq
, т.е. «петух» (на латыниgallus ). Буабодран как бы ненароком увековечил свое имя в названии нового элемента.
Изучая полученный галлий, Буабодран определил, что плотность отличается от предсказанной Менделеевым. Когда Менделеев узнал об этом, то написал французскому коллеге с рекомендацией . И как оказалось, не напрасно: первые данные Буабодрана действительно были неверными.
Понятие легкоплавких металлов/сплавов
Легкоплавкость – понятие растяжимое, особенно это актуально для промышленности. В химии легкоплавкими считаются элементы группы металлов + их сплавы, температура плавления которых ниже порога в 1000 градусов Цельсия.
Если температура плавления металла превышает 1 500 градусов Цельсия – его принято выделять в группу тугоплавких. Диаграмма выше четко дает понять, куда какой металл следует относить.
Теперь пройдемся по легкоплавким сплавам. В своем большинстве – это сплавы эвтектического типа, пиковая температура плавления которых не превышает 232 градусов по Цельсию. В основе производства легкоплавких сплавов лежат легкоплавкие металлы – олово, висмут, таллий, галлий и другие.
Ученым удалось добиться -78 градусов в качестве минимальной температуры плавления для советского сплава, который состоит на 12% из натрия, 47% калия и 41% цезия. Недостаток сплава — реакция с водой. Ближайший конкурент – амальгама. Токсичный сплав из ртути с таллием, сохраняющий жидкое состояние до температуры -61 градус по Цельсию.
Область применения легкоплавких металлов/сплавов:
- энергетическая промышленность и машиностроение. Основное направление – создание тепловых носителей с жидкометаллического типа;
- литьевая промышленность;
- как основа для датчиков температуры, что актуально в системах пожарной безопасности;
- как основа для разработки термометров;
- как ремонтный материал в вакуумных технологиях;
- припои, предохранители и прочие мелочи в микроэлектронике;
- медицинское направление. То же протезирование;
- как металлическая смазка.
Низкая температура плавления является базовых свойством, которое требуется от легкоплавких металлов и сплавов
Вторичные параметры, которые берутся во внимание в различных областях использования – плотность, прочность на разрыв и инертность в химическом плане
Какие есть технологии плавления металлов в домашних условиях?
при работе с куклами все чаще сталкиваюсь с потребностью в необычных металлических деталях.поэтому возник вопрос есть ли технологии какие то позволяющие делать какие-то сплавы в домашних условиях?и какие есть варианты изготовления молдов?силиконовые я так понимаю до 250 температуру выдерживают
ой, бросьте на это заморачиваться, на это жизнь надо положить
а так -ну, моделирование из воска, перевод в выплавляемые модели, формомасса(какие такие молды), прокалка в печке, металл поплавили и лить. всё понятно? ну потом там подработаете немножко, плёвое дело, я тут писала про шлифовки-полировки, ерунда
плавка -это самое простое, приличная горелка нужна, в готовые опоки вы спокойно отольете гидроударом дома на столе. только где их взять готовые как хочется.
ну а если серьёзно, мне кажется, для декоративных целей гальваника очень хорошо смотрится, но я не спец в этой теме
SilverClay? Бывает и медная, кажется. Или слепить из пластики и покрасить “металлической” краской?
я металлклэй пробовала во многих вариантах и мое мнение как керамиста и ювелира -неудачный материал , да и на коленке особо не сляпать, нужна как минимум горелка, а лучше печка. а при таком оборудовнии уже лучше делать как положено из нормального из металла, так думаю
Из простого сплав розе(вуда) температура плавления около 100 градусов – купить можно в магазине радиодеталей.
дальше уже идет олово температура 240. все что с температурой выше лучше дома не заниматься.
да мало ли что есть низкоплавкое по сплавам. но там задача -сделать украшение. уж как там делать -непонятно, толи лить, толи так руками кромсать. лучше вообще не делать из непоняток, там никто не подскажет, не поможет.
вы что, прольёте вышеупомянутые сплавы? вы знаете, как их паять?
и про температуру дома не заниматься -да ладно, приходится заниматься.
что -то вы в заблуждение вводите девочек
А что в них непроливаемого ? сплав розе отлично проливается, не прольется можно еще добавить литье на “хлопок” описанный выше – там уж точно все прольется.
Да в чем заблуждение то – солдатиков в силикон давно уже льют.
если далеко не ходить – в гугле достотчно много примеров по тем же солдатикам (ссылки не могу публиковать).
Понятно что приходится, только если серьезные сплавы ( >1000C) лить там ведь и готовиться приходиться по другому.
А если человеку попробовать хочется, процесс литья же интересный – так что думаю для начала оптимально.
я просто не знаю про такие сплавы, прольется-ну и славно. обычно металл так сам по себе не проливается, его приходится подпихивать в дыру
ну и моделирование под металл тоже довольно специфично, скорее всего готовые молды не прокатят
Чтоб розе хорошо пролился, достаточно массивного литника, который и создаст нужное давление. Лила фигурки в силикон, с графитной смазкой. Проблем не было ни разу.
Другое дело, что бижу я бы из него делать не стала – все равно окисляется и пачкается. Как вариант – последующая гальваника. Но не знаю ляжет ли та же медь на олово.
Представление о технологии можно получить, а так самое простое помоему – если в литье не втягиваться, сделать восковки и отдать лить на сторону из нормальных металлов.
вот да. ну не прольете вы дома на коленке нормальный металл. я пролью, но не надо так надрываться, лучше отдать литейку на сторону
в крайне случае наберите в поиске литье по вашим моделям
подпихивать литейку в дыру -это гидроудар, центробег или вакуум. оптимально конечно вакуум
гидроудар спокойно на коленке можно сделать, картошку режете и ей затыкаете опоку. можно глиной заткнуть, но у вас глины нет, а у меня её навалом любая
Можно еще методом обратной заливки )
тут хотят попростому металл отлить, а это на мой взгляд нереально
если что -я свой ювелирный диплом в пту делалала дома на столе литьем гидроударом в готовую китайскую опоку в серебре . надо будет -и проплавишся и прольешся
Натрий (97,8°C)

При этом выделяется много тепла, которое тут же поджигает освободившийся водород. Взрыв и пожар! Такие материалы как натрий хранят в керосине, что исключает их контакт с водой и влагой воздуха.
Как очень активный элемент, натрий в том или ином виде присутствует вокруг нас в огромных количествах. Взять хотя бы хлорид натрия — обычная поваренная соль.
Чем опасна нехватка витамина Д?
Запасы восполняются за счет ежедневного пребывания на солнце, в этом случае его нехватка возникает редко.
Как составляющая всех жизненно важных систем детского организма, недостаток такого витамина может привести к осложнениям в виде нарушения в развитии опорно-двигательного аппарата, костной и нервной системы. Самые безобидные последствия, когда витамин Д для грудничков вырабатывается ниже нормы, – это потеря сна и аппетита, расстройства ЖКТ, апатия или повышенная возбудимость, сильное потоотделение, частые простудные заболевания.
К более серьезным заболеваниям относят рахит. Авитаминоз (катастрофическая нехватка витамина Д) препятствует усвоению кальция (наблюдают вторичный гиперпаратиреоз) и выведению фосфата посредством мочеиспускания.
Рахит проявляется:
- замедлением прорезывания и роста зубов;
- слабым зарастанием (не зарастанием) родничка;
- снижением тонуса мышц;
- размягчением плоских черепных костей и уплощением затылка;
- деформацией лицевой части черепа («Седловидный нос», «Высокое готическое небо»);
- формированием наслоений на теменном и лобном буграх («Лоб Сократа», «Квадратная голова»);
- изменением формы грудины («Куриная грудь»);
- искривлением нижних конечностей;
- искажением костей таза («Плоский таз»).
Использование самого легкоплавкого металла в медицине
Ядовитый металл чаще всего встречался в эликсирах бессмертия и лекарствах для продления жизни. Алхимики пробовали добывать золото прямо из ртути, только сначала ее надо было нагреть. Ртуть называли праматерью металлов, она входила в теорию трех начал (с серой и солью) и была основным элементом философского камня.
Даже магические действия шаманов не могли обойтись без ртути. Распыляемым порошком киновари отпугивали нечистых духов. Несмотря на токсичность, «серебряную воду» активно использовали древние врачи практически во всех сферах своей деятельности.
Древнеегипетские жрецы клали немного ртути в сосуд и помещали в горло фараона, чтобы обезопасить его в загробной жизни.
Врачи были уверены, что жидкое серебро должно замечательно проходить сквозь человеческие кишки, распрямляя их. Но данный способ почему-то не прижился, так как у пациентов от большого объема высокоплотного «лекарства» происходил разрыв желудка.
Утверждают, что Иван Грозный стал жертвой именно ртути. Предположительно, ему или лечили сифилис, или давали лекарства, содержащие ртуть. То, что русский царь умер в результате ртутной интоксикации и имел деформации костей, свойственные глубоким старикам, уже доказано несколькими учеными.
Историки отмечали, что перед смертью царь очень изменился. Постоянная свирепость, искаженные черты лица, на теле не осталось ни единого волоса. Постоянные эпилептические припадки служили очередным доказательством отравления.
В 70-х годах в продаже можно было встретить множество препаратов с ртутью: мочегонные, слабительные, в мазях для отбеливания лица и антисептиках.
Амальгама серебра не так давно была распространенным пломбировочным стоматологическим материалом в России и до сих пор используется в дешевых пломбах за рубежом.
Самый легкоплавкий металл на планете необходим человечеству по-прежнему. А вот смогут ли люди дружить с ним, не отравляя жизнь вокруг — очень спорный вопрос…
Вольфрам
Самая высокая температура плавления — у металла вольфрама. Выше него по этому показателю стоит только неметалл углерод. Вольфрам представляет собой светло-серое блестящее вещество, очень плотное и тяжелое. Он кипит при 5555 °C, что почти приравнивается к температуре фотосферы Солнца.
При комнатных условиях он слабо реагирует с кислородом и не подвергается коррозии. Несмотря на свою тугоплавкость, он довольно пластичен и поддается ковке уже при нагревании до 1600 °C. Эти свойства вольфрама используют для нитей накаливания в лампах и кинескопах электродов для сварки. Большую часть добытого металла сплавляют со сталью, чтобы повысить ее прочность и твердость.
Широкое применение вольфрам имеет в военной сфере и технике. Он незаменим для изготовления боеприпасов, брони, двигателей и наиболее важных частей военного транспорта и самолетов. Из него также делают хирургические инструменты, ящики для хранения радиоактивных веществ.

Примерная программа упражнений на неделю
Составив недельный план занятий для развития трехлетнего ребенка, вы сможете равномерно распределить занятия по дням недели, при этом ничего не упускать, но и не перегрузить карапуза. Для каждого ребенка такой план занятий будет своим. Его составление должно быть основано на интересах малыша и мамы, а также наличии определенных навыков у карапуза. В план вписывается посещение спортивных и развивающих занятий, массаж и другие обязательные действия.
При составлении плана впервые лучше ориентироваться на минимальный перечень занятий. Через одну-две недели вы сможете проанализировать, как ребенок справляется, нужно ли добавить какие-либо занятия, что больше нравится малышу, а что удается сложнее.
Мы предлагаем такой примерный недельный распорядок развивающих занятий для 3-летнего ребенка:
|
Понедельник |
Вторник |
Среда |
Четверг |
Пятница |
Суббота |
Воскресенье |
|
|
Физическое развитие |
Плавание |
Зарядка по видео-уроку |
Игры с мячом |
Прыжки |
Зарядка под музыку |
Игра с фитболом |
Подвижные игры |
|
Познавательное развитие |
Изучение цифр |
Изучаем птиц |
Пазлы |
Ищем целое по детали |
Лото |
Изучение явлений природы |
Изучение цветов |
|
Сенсорное развитие |
Игры с сенсорным мешочком |
Изучаем вкусы |
Изучаем запахи |
Угадывание предметов на ощупь |
|||
|
Мелкая моторика |
Пальчиковая гимнастика |
Игра с прищепками |
Игра с песком |
Игра с бусинами |
Мозаика |
Игра с водой |
Игра с крупой |
|
Музыкальное развитие |
Танцы |
Пение |
Изучение музыкальных инструментов |
Музыка фоном |
|||
|
Речевое развитие |
Чтение сказки |
Артикуляционная гимнастика |
Рассказываем сказку по картинке |
Разучиваем стих |
Аудио-сказка |
Загадки |
Обсуждаем сюжет картинки |
|
Творческое развитие |
Лепка |
Рисование |
Кукольный театр |
Рисование |
Игры с конструктором |
Раскрашивание |
Аппликация |
|
Социальное развитие |
Изучаем этикет |
Игры со сверстниками |
Изучаем слова вежливости |
Оборудование и материалы, которые понадобятся
Для того, чтобы произвести плавку металла необходимо купить следующие компоненты для изготовления:
- огнеупорный кирпич;
- гвозди;
- трансформатор;
- медный провод;
- графит;
- слюда;
- асбестовые и цементные плитки;
- газовая горелка;
- тигель.
Размеры будут варьироваться от желания собирающего ее. Лучше создать небольшую печь для переплавки металлов, если вы хотите ее использовать только для своих нужд. Вы потратите меньше времени на ее изготовление, и на разогрев ее будет тратиться малое количество киловатт. Если вы делаете ее на солярке или на угле, то не забудьте про установку теплоизоляции и поддува воздуха.
В электропечи плавятся такие металлы, как железо, никель, олово, медь. Напряжение на выходе в электропечи должно быть больше, а значит и расстояние между электродами будет увеличиваться. Щетки от электромотора подойдут вместо электродов.
Свойства галлия
Галлий – мягкий пластичный металл серебристого цвета. При низких температурах находится в твердом состоянии, но плавится уже при температуре, ненамного превышающей комнатную (29,8°C).
Вообще широкий температурный интервал существования жидкого состояния этого металла (от 30 и до 2230 °C) является одной из особенностей галлия. Химические свойства галлия близки к свойствам алюминия. В связи с легкоплавкостью, перевозка галлия осуществляется в полиэтиленовых пакетах.
До появления полупроводников, галлий использовался для создания легкоплавких сплавов. Сегодня же галлий используется, главным образом, в микроэлектронике в составе полупроводников. Нитрид галлия используется в создании полупроводниковых лазеров и светодиодов синего и ультрафиолетового диапазона.
Галлий — превосходный смазочный материал. На основе галлия и никеля, галлия и скандия созданы очень важные в практическом плане металлические клеи. Металлическим галлием также заполняют кварцевые термометры для измерения высоких температур, заменяя этим металлом ртуть. Это связано с тем, что галлий имеет значительно более высокую температуру кипения по сравнению с ртутью.
Галлий — один из самых дорогих металлов. Так в 2005 году на мировом рынке тонна галлия стоила 1,2 млн долларов США
В связи с его высокой стоимостью и с большой потребностью в этом металле, очень важно наладить его полное извлечение при алюминиевом производстве и переработке каменных углей на жидкое топливо
Плавка металла и чугуна
Печь для плавки металла представляет собой корпус, изготовленный из шамотного кирпича. Связующим элементом является глина. Топка предназначена для горения угля. Снизу предусматривается отверстие, через которое ведется наддув в пекло. Внизу размещается чугунная решетка, которая называется колосником. На ней выкладывается кокс или уголь. Его можно снять со старой печи. Иногда огнеупорный кирпич, при формировании корпуса, укладывается на ребро. Готовая конструкция скрепляется снаружи металлическим поясом.
Печь для переплавки металлов должна иметь тигель. Это может быть эмалированный или чугунный казанок. Месторасположение тигля — рядом с горящим коксом. С целью улучшения поддува рядом устанавливают вентилятор. Оборудование применяется для выплавки стали, но можно использовать как печь для выплавки чугуна.
Интересные опыты с галлием
о
Довольно увлекательный эксперимент можно провести с затвердеванием галлия. Представленный металл имеет свойство расширяться в ходе затвердевания. Для проведения интересного опыта достаточно поместить жидкий галлий в стеклянный пузырек. Далее необходимо начать охлаждать емкость. Через некоторое время можно заметить, как в пузырьке станут образовываться кристаллы металла. Они будут иметь синеватый цвет, в отличие от серебристого оттенка, который характерен для материала в жидком состоянии. Если не прекращать охлаждение, кристаллизирующийся галлий в конечном итоге разорвет стеклянный пузырек.
Свойства
Чтобы понимать, где лучше использовать материал, нужно знать свойства тугоплавких металлов. Из них изготавливаются детали для промышленного оборудования, техники и электроники. Характеристики тяжелых тугоплавких металлов будут описаны ниже.
Физические свойства
Характеристики:
- Плотность — до 10000 кг/м3. У вольфрама этот показатель достигает 19000 кг/м3.
- Средняя температура плавления — 2500 градусов по Цельсию. Самая высокая температура плавления металла у вольфрама — 3390 градусов.
- Удельная теплоёмкость — 400 Дж.
Тугоплавкие предметы не выдерживают ударов и падений.
Химические свойства
Химические свойства:
- Это твердые вещества, обладающие высокой химической активностью.
- Прочная межатомная структура.
- Сопротивляемость длительному воздействию кислот и щелочей.
- Высокий показатель парамагнитности.
Эти материалы имеют некоторые недостатки. Главным из них является трудный процесс обработки и изготовления продукции из него.
4. Хром

Хром ценится за высокую коррозионную стойкость и твердость. С ним легче обращаться, чем с металлами платиновой группы, к тому же он более распространен, поэтому хром является популярным элементом, используемым в сплавах, таких, как нержавеющая сталь.
А еще один из прочнейших металлов на Земле используется при создании диетических добавок. Конечно, вы будете принимать внутрь не чистый хром, а его пищевое соединение с другими веществами (например, пиколинат хрома).
Суть понятия самого легкоплавкого металла
Для специалистов больше знакомо понятие «тугоплавкость». Хотя слово «легкоплавки» и является антонимом в языковом аспекте, на практике – это один из пунктов к общей классификации в промышленности. По своей сути, любой элемент, имеющий температуру плавления менее 600 градусов по Цельсию, называют легкоплавким. Некоторые источники ставят планку вхождения в группу еще ниже – до 500 градусов Цельсия.
Классификация металлов по плавкости:
- легкоплавкие. Температура плавления элементов обязана быть ниже 600 градусов по Цельсию;
среднеплавкие металлы. Чтобы материал расплавился, потребуется температура от 600 до 1600 градусов со значением плюс;
тугоплавкие. Металлические вещества с порогом плавления выше 1 600 градусов по Цельсию.
Процесс плавления одинаковый для всех металлических элементов – либо внешнее воздействие, либо внутреннее. В первом случае – это расплавка в печах, а во втором – разогревание через пропуск электрического тока сквозь металл. Иногда используется индукционный нагрев в электромагнитном поле с высокой частотой.
Процесс плавки металла через призму науки:
- Разогрев до температуры плавления.
- Увеличение амплитуды тепловых колебаний молекул внутри металла.
- Возникновение дефектов в структуре решетки материала.
- Межатомные связи разрываются + параллельно затрачивается энергия.
- Образование на поверхности квазижидкого слоя.
- Постепенное разрушение решетки и накопление дефектов, что и принято называть процессом плавления.
В зависимости от температуры плавления, выбирают аппараты из сплавов, способных выдержать пиковые значения. Для легкоплавких металлов вопрос решается проще всего.
Второй весомый параметр – температура кипения металла. В 95% случаев она в 2 раза выше температуры плавления. Между собой эти две величины являются прямо пропорциональными + при снижении/увеличения давления на материал, снижается и его показатели плавления с кипением.
Муфельная печь
Муфельные печи часто используются для термообработки деталей. Такое оборудование характеризуется большим температурным диапазоном, от 20 до 1000 градусов.
Муфельная печь для закалки металла работает на разных видах энергии. Однако в домашних условиях лучше применять агрегат, работающий на электроэнергии. Закаливание ведется в муфеле печи.
Муфельная печь своими руками изготавливается за несколько этапов:
- Изготовление муфеля ведется из шамотного кирпича. Из-за круглой формы корпуса печи, у них скашиваются углы. В каждом кирпиче выбираются канавки, куда ведется закладка спирали.
- Если муфельная печь для плавки изготавливается из духовки, то внутри она обкладывается огнестойким кирпичом. В кладке прорезаются канавки для спирали.
- Изготовленная из огнеупорного кирпича камера, помещается в корпус, сделанный из стали. На дно укладывается изоляция. Зазор между боковыми стенками камеры и корпуса составляет 4 см, куда вставляется утеплитель. Верх состоит из 2 слоев металла и утеплителя.
- В корпусе сверлятся отверстия, и через них выводятся концы спирали, которые подключаются к сетевому кабелю.
- В случае использования духовки, утеплитель не требуется. Он в ней уже предусмотрен.
Области применения галлия
Бóльшая часть добываемого галлия используется для производства полупроводников. Арсенид (GaAs) и нитрид галлия (GaN) используются в электронных компонентах многих устройств, для создания интегральных схем, высокопроизводительных процессоров, микроволновых усилителей. Арсенид галлия используется в различных электрооптических инфракрасных приборах. Арсенид галлия-алюминия применяется для создания инфракрасных лазерных диодов высокой мощности. На основе нитрида галлия и нитрида индия-галлия производят синие и фиолетовые лазерные диоды. Кстати, лазер на нитриде галлия применяется в приводах Blu-ray дисков.
Фотоэлементы на основе арсенида галлия, фосфида и арсенида индия-галлия установлены на космических спутниках и марсоходах.
Галлий имеет интересную особенность: он сильно понижает температуру плавления сплавов, в которых содержится. При этом температура опускается ниже, чем у каждого компонента сплава по отдельности (эвтектические составы). Так, сплав Галинстан (68,5 % галлия, 21,5 % индия и 10 % олова) имеет температуру плавления -19 °С и используется в некоторых термометрах вместо ртути.
Галлий применяется и в медицине. В целом металл характеризуется низкой токсичностью и не выполняет естественной биологической функции. Поэтому препараты на основе галлия могут применяться при лечении и диагностике раковых заболеваний (изотопы галлий-67 и -68). Также галлий используется при лечении некоторых бактериальных инфекций: ион Ga³⁺ замещает Fe³⁺ в метаболических путях дыхания бактерий, вызывая их гибель. Препараты на основе галлия могут применяться при лечении малярии.
Еще галлий помогает обнаружить нейтрино-частицы, исходящие от Солнца. Как правило, выявление таких частиц — это весьма сложный и трудоемкий процесс. Галлий в составе регистрационной смеси повышает чувствительность анализа, а соответственно, и помогает зафиксировать нейтрино. Детекторы GALLEX Национальной лаборатории Гран-Сассо содержат 12,2 тонны галлия-71. Они улавливают нейтрино, исходящие от Солнца, и превращают его в радиоактивный изотоп, излучение которого можно зафиксировать. Подобные исследования также проводят в Баксанской нейтринной обсерватории (Кабардино-Балкария), где нейтрино-детекторы содержат 5 тонн жидкого галлия.
По температуре плавления галлия можно проверять термометры! Эта величина — 302,9146 K (29,7646 °C) – признана стандартом Международного бюро мер и весов.
В 2007 году с помощью пучков ионов галлия толщиной 7 нм в Simon Fraser University напечатали самую маленькую в мире книгу – Teeny Ted from Turnip Town. Книга получилась размером 0,07x 0,10 мм.
У галлия есть еще одно забавное применение: ложки из галлия, по виду не отличимые от алюминиевых, используют для фокуса с исчезающей ложкой. В горячем чае или кофе такая ложка попросту расплавится!
- Paul Parsons, Gail Dixon — The Periodic Table A visual guide to the elements (p.78);
- Wikipedia.Gallium;
- Wikipedia.Gallex;
- Wikipedia. Teeny_Ted_from_Turnip_Town.
В заключение
Вот мы и выяснили, какой металл плавится в руке. Сегодня галлий можно отыскать в продаже для проведения собственных опытов
Однако обращаться с материалом следует крайне осторожно. Твердый галлий является нетоксичным веществом
Однако продолжительный контакт с материалом в жидкой форме может привести к самым непредвиденным последствиям для здоровья, вплоть до остановки дыхания, паралича конечностей и вхождения человека в состояние комы.
Галлий – это химический элемент из 3 группы периодической системы Менделеева. Он имеет порядковый номер 31, атомную массу 69,72, обозначается значком Ga и обладает серебристо-белым мягким металлическим цветом. Добывают галлий только преимущественно из цинковых руд и бокситов, в чистом виде его не существует. Но что удивительно для простого обывателя, это то, что имея очень низкую температуру для плавления, можно собственными глазами, не в лабораторных условиях, увидеть, как металл буквально растает в руках, словно снег. Галлий плавится при 29,8°C.
Кому же он может пригодиться такой? Может и многим. Несмотря на его таяние, галлий широко применяют в микроэлектронике, а начиная с 1875 года, когда его впервые открыли, с помощью такого металла создавали легкоплавкие сплавы. Сейчас химическое соединения «Галлия», именуемое Арсенид галлия (GaAs) используется в инфракрасных приложениях и микроволновых схемах. А вот в современных лазерах, различных светодиодах голубого и ультрафиолетового света используют другое соединение металла — нитрид галлия.
Широко применяют его в медицине, так как было установлено, что частицы галлия способны заменить частички железа, необходимые для функционирования организма. А также его включают в состав различных медицинских препаратов. Металлическим галлием, кроме всего, заполняют кварцевые термометры для измерения высоких температур, заменяя им привычную нам ртуть. Связано это с тем, что по сравнению с ртутью металл имеет очень высокую температуру кипения.
Для человека прямой контакт с металлом губителен. Острое отравления можно определить по таким признакам: кратковременное возбуждение, арефлексия, заторможенность, адинамия, нарушение координации движений, замедление и нарушение ритма дыхания. И параллельно со всем этим наступает паралич нижних конечностей, а в итоге – кома и смерть.
Считается он и очень дорогим металлом на мировом рынке. Например, по данным 2005 года одна тонна металла стоила 1,2 миллиона долларов США. Разумеется, научный прогресс не стоит на месте, и наиболее широко сейчас стоит вопрос о том, чтобы извлекать галлий при создании жидкого топлива из каменного угля.


 Направляющие тормозного суппорта: как и чем смазывать
Направляющие тормозного суппорта: как и чем смазывать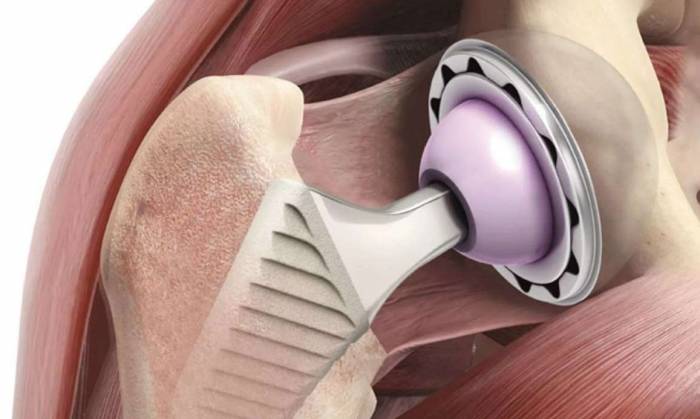 Операция по замене тазобедренного сустава - показания, виды эндопротезов
Операция по замене тазобедренного сустава - показания, виды эндопротезов Ортез на коленный сустав orlett hks-303
Ортез на коленный сустав orlett hks-303















 Имплант тазобедренного сустава zimmer
Имплант тазобедренного сустава zimmer Как делать маникюр по фен-шуй и какие пальцы красить
Как делать маникюр по фен-шуй и какие пальцы красить